дә§е“Ғд»Ӣз»Қпјҷь/div>
еҹәжң¬дҝЎжҒҜ
| еҲҶеӯҗејҺь/td> |
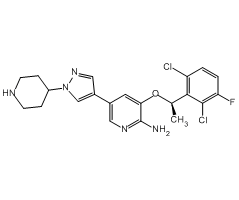
C21H22Cl2FN5O |
| еҲҶеӯҗйҮҺь/td> |
450.34 |
| еӯҳеӮЁжқЎд»¶ |
Freezer -20в„Ӯь/td> |
дә§е“ҒжҸҸиҝ°
Crizotinib (PF-02341066) е…Ӣе”‘жӣҝе°јжҳҜдёҖз§Қжңүж•Ҳзҡ„c-Metе’ҢALKжҠ‘еҲ¶еүӮпјҢеңЁз»ҶиғһиҜ•йӘҢдёӯIC50еҲҶеҲ«дё?1 nM е’ 24 nMгҖӮе®ғеҗҢж—¶д№ҹжҳҜжңүж•Ҳзҡ„ROS1жҠ‘еҲ¶еүӮпјҢе…¶KiеҖје°Ҹдә?.025 nMгҖҒь/p>
йқ¶зӮ№пјҲIC50 & TargeпјҲь/b>
ALK,24 nM (cell free)
c-Met,11 nM (A498 cells)
дҪ“еӨ–з ”з©¶
PF-2341066дҪңз”ЁдәҺmIMCD3е°Ҹйј е’ҢMDCKзҠ¬дёҠзҡ®з»ҶиғһпјҢдҪңз”ЁдәҺc-MetзЈ·й…ёеҢ–дҪңз”Ёж—¶е…·жңүзӣёдјјж•ҲжһңпјҢIC50еҲҶеҲ«дё? nM е’?0 nMгҖӮPF-2341066дҪңз”ЁдәҺиЎЁиҫҫc-Met ATP-з»“еҗҲдҪҚзӮ№зӘҒеҸҳеһӢV1092I жҲ–H1094RжҲ P-зҺҜзӘҒеҸ M1250T зҡ„NIH3T3 з»ҶиғһпјҢе…·жңүзӣёдјјзҡ„жҙ»жҖ§пјҢдё”жҙ»еҠӣеўһй«ҳпјҢIC50еҲҶеҲ«дё?9 nM,2 nM е’?5 nM,иҖҢдҪңз”ЁдәҺиЎЁиҫҫйҮҺз”ҹеһӢеҸ—дҪ“зҡ„NIH3T3 з»Ҷиғһж—¶пјҢIC50дё?3 nMгҖӮ[1] зӣёеҸҚ, и§ӮеҜҹеҲ°PF-2341066дҪңз”ЁдәҺиЎЁиҫҫc-Metжҙ»еҢ–зҺҜзӘҒеҸҳеһӢY1230C е’ҢY1235Dзҡ„з»Ҷиғһж—¶пјҢдёҺдҪңз”ЁдәҺйҮҺз”ҹеһӢеҸ—дҪ“зӣёжҜ”пјҢж•ҲжһңеҸ‘з”ҹжҳҫи‘—ж”№еҸҳпјҢIC50еҲҶеҲ«дё?27 nM е’?2 nMгҖӮPF-2341066 дҪңз”ЁдәҺеҲҶеҲ«иЎЁиҫҫеҶ…жәҗжҖ§c-Met зӘҒеҸҳдҪ“R988Cе’ T1010I зҡ„NCI-H69 е’ҢHOP92 з»ҶиғһпјҢд№ҹжңүж•ҲжҠ‘еҲ¶c-Met зЈ·й…ёеҢ? IC50еҲҶеҲ«дё?3 nM е’?6 nMгҖӮдёҺдҪңз”ЁдәҺc-MetзӣёжҜ”пјҢPF-2341066дҪңз”ЁдәҺVEGFR2 е’ҢPDGFRҰВ RTKs, йҖүжӢ©жҖ§й«ҳ1000еӨҡеҖҚпјҢдҪңз”ЁдәҺIRKе’ҢLckйҖүжӢ©жҖ§й«ҳ250еӨҡеҖҚпјҢдҪңз”ЁдәҺTie2, TrkA,е’ҢTrkBйҖүжӢ©жҖ§й«ҳ40еҲ?0еҖҚгҖӮPF-2341066 дҪңз”ЁдәҺRONе’ Axl RTKsж—¶йҖүжӢ©жҖ§дёә20еҲ?0еҖҚгҖӮзӣёеҸҚпјҢPF-2341066 дҪңз”ЁдәҺиЎЁиҫҫALK RTK зҡ„ж ёзЈ·иӣӢзҷ (NPM)- й—ҙеҸҳжҖ§ж·Ӣе·ҙзҳӨжҝҖй…?ALK) иҮҙзҷҢиһҚеҗҲзӘҒеҸҳдҪ“е’Ң KARPAS299дәәй—ҙеҸҳжҖ§еӨ§з»Ҷиғһж·Ӣе·ҙзҳ?ALCL)з»Ҷиғһзі»ж—¶е…·жңүзӣёиҝ‘зҡ„IC50еҖјпјҢдё?4 nMгҖӮPF-2341066жҠ‘еҲ¶c-Metдҫқиө–зҡ„зҷҢз»Ҷиғһзҡ„иӮҝзҳӨиЎЁзҺ°еһӢпјҢе’ҢеҶ…зҡ®з»Ҷиғһзҡ„иЎҖз®Ўз”ҹжҲҗиЎЁзҺ°еһӢгҖӮPF-2341066жҠ‘еҲ¶дәәGTL-16иғғзҷҢз»Ҷиғһз”ҹй•ҝпјҢIC50дё?.7 nMгҖӮPF-2341066иҜұеҜј GTL-16з»ҶиғһеҮӢдәЎпјҢIC50 дё?.4 nMгҖӮPF-2341066 жҠ‘еҲ¶HGFеҲәжҝҖзҡ„дәәNCI-H441иӮәзҷҢз»ҶиғһиҝҒ移е’Ңе…ҘдҫөпјҢIC50еҲҶеҲ«дё?1 nM е’?.1 nMгҖӮPF-2341066жҠ‘еҲ¶ MDCKз»Ҷиғһж•Је°„пјҢIC50дё?6 nMгҖӮPF-2341066 жҠ‘еҲ¶HGF-еҲәжҝҖзҡ„c-MetзЈ·й…ёеҢ?з»Ҷиғһеӯҳжҙ»пјҢе’ҢMatrigelе…ҘдҫөпјҢIC50еҲҶеҲ«дё?1 nM, 14 nMе’?5 nMгҖӮжӯӨеӨ? PF-2341066жҠ‘еҲ¶зәӨз»ҙиӣӢзҷҪиғ¶дёӯзҡ„иЎҖжё…еҲәжҝҖзҡ HMVECеҲҶж”Ҝе°Ҹз®ЎеҪўжҲҗ (еҪўжҲҗиЎҖз®?гҖӮ[1] PF-2341066 дҪңз”ЁдәҺKarpas299 жҲ–SU-DHL-1 ALCLз»ҶиғһпјҢд№ҹжңүж•ҲжҠ‘еҲ¶ NPM-ALKзЈ·й…ёеҢ–пјҢIC50 дё?4 nMгҖӮPF-2341066 жңүж•ҲжҠ‘еҲ¶з»Ҷиғһеўһж®–пјҢдјҙйҡҸзқҖдҪҝз»Ҷиғһе‘ЁжңҹеҒңеңЁG(1)-SжңҹпјҢдё”иҜұеҜ ALKйҳіжҖ§зҡ„ ALCL з»ҶиғһеҮӢдәЎпјҢIC50дё?0 nM, дҪҶжҳҜдҪңз”ЁдәҺALKйҳҙжҖ§зҡ„ж·Ӣе·ҙзҳӨз»ҶиғһеҲҷж— ж•ҲжһңгҖ [2] жӯӨеӨ–, PF-2341066 жҠ‘еҲ¶йӘЁиӮүзҳӨзҡ„дёҖдәӣжҙ»еҠЁиЎҢдёәпјҢеҸҠе…¶иӮҝзҳӨз”ҹй•ҝ (дҫӢеҰӮ,еўһж®–е’Ңеӯҳжҙ?е’ҢиҪ¬з§ (дҫӢеҰӮпјҢе…Ҙдҫөе’ҢеҪўжҲҗе…ӢйҡҶ)гҖӮ[3]
дҪ“еҶ…з ”з©¶
PF-2341066жҜҸеӨ©жҢ?0 mg/kgе’?5 mg/kgеүӮйҮҸеӨ„зҗҶGTL-16 жЁЎеһӢ, еј•иө·еӨ§иӮҝзҳ (дҪ“з§ҜеӨ§дәҺ600 mm3) жҳҺжҳҫиЎ°йҖҖпјҢдё”жҢ?3еӨ©еӨ„зҗҶж—ҘзЁӢеӨ„зҗҶеҗҺпјҢе№іеқҮиӮҝзҳӨдҪ“з§ҜйҷҚдҪ?0%гҖӮеңЁеҸҰдёҖйЎ№з ”з©¶дёӯ, PF-2341066еӨ„зҗҶ3дёӘжңҲд»ҘдёҠпјҢе®Ңе…ЁжҠ‘еҲ¶GTL-16иӮҝзҳӨз”ҹй•ҝпјҢPF-2341066жҜҸеӨ©жҢ?0 mg/kgеүӮйҮҸеӨ„зҗҶе°Ҹйј пј?дёӘжңҲеҗҺпјҢеҸӘжңү1/12е°Ҹйј зҡ„иӮҝзҳӨз”ҹй•ҝеҫ—еҲ°жҸҗй«ҳгҖӮPF-2341066жҜҸеӨ©жҢ?0 mg/kgеүӮйҮҸеӨ„зҗҶNCI-H441 NSCLC жЁЎеһӢеӨ„зҗҶе‘Ёжңҹдё?8еӨ©пјҢи§ӮеҜҹеҲ°е№іеқҮиӮҝзҳӨдҪ“з§ҜйҷҚдҪ?3%гҖӮPF-2341066 жҜҸеӨ©жҢ?0 mg/kgеүӮйҮҸдҪңз”Ёдә Caki-1 RCCжЁЎеһӢпјҢеӨ„зҗҶе‘Ёжңҹдёә33еӨ©пјҢи§ӮеҜҹеҲ°е№іеқҮиӮҝзҳӨдҪ“з§ҜйҷҚдҪ?3%пјҢдё”жҜҸз§ҚиӮҝзҳӨдҪ“з§ҜйҷҚдҪҺиҮіе°‘30%гҖӮPF-2341066жҜҸеӨ©жҢ 50 mg/kgеүӮйҮҸдҪңз”Ёдә U87MG жҒ¶жҖ§иғ¶иҙЁзҳӨжҲ–PC-3еүҚеҲ—и…әзҷҢ移жӨҚзҳӨжЁЎеһ?еҮ д№Һе®Ңе…ЁжҠ‘еҲ¶иӮҝзҳӨз”ҹй•ҝпјҢеңЁе®һйӘҢжңҖеҗҺдёҖеӨ©пјҢжҠ‘еҲ¶еҲҶеҲ«иҫ?7% жҲ?4%гҖӮзӣёеҸ? PF-2341066жҜҸеӨ©жҢ?0 mg/kgеүӮйҮҸеҸЈжңҚз»ҷиҚҜеӨ„зҗҶ MDA-MB-231 д№іи…әзҷҢжЁЎеһ?жҲ DLD-1 з»“иӮ зҷҢжЁЎеһӢпјҢдёҚдјҡжҳҫи‘—жҠ‘еҲ¶иӮҝзҳӨз”ҹй•ҝгҖӮPF-2341066жҜҸеӨ©жҢ?2.5 mg/kg, 25 mg/kg, е’?0 mg/kgеүӮйҮҸдҪңз”Ёдә GTL-16 иӮҝзҳӨпјҢи§ӮеҜҹеҲ°CD31йҳіжҖ§еҶ…зҡ®з»Ҷиғһжҳҫи‘—йҷҚдҪҺпјҢиҝҷз§ҚдҪңз”ЁеӯҳеңЁеүӮйҮҸдҫқиө–жҖ§пјҢиҜҙжҳҺ MVD еҸ—жҠ‘еҲ¶пјҢдё”е…·жңүзӣёе…ізҡ„жҠ—зҷҢй«ҳж•ҲжҖ§пјҢиҝҷз§ҚдҪңз”Ёд№ҹеӯҳеңЁеүӮйҮҸдҫқиө–жҖ§гҖӮPF-2341066 дҪңз”ЁдәҺGTL-16 е’ U87MG жЁЎеһӢпјҢжҳҫи‘—йҷҚдҪҺдәәVEGFA е’ҢIL-8иЎҖжөҶж°ҙе№іпјҢиҝҷз§ҚдҪңз”ЁеӯҳеңЁеүӮйҮҸдҫқиө–жҖ§гҖӮPF-2341066еҸЈжңҚеӨ„зҗҶGTL-16 иӮҝзҳӨпјҢи§ӮеҜҹеҲ°зЈ·й…ёеҢ–зҡ„c-Met, Akt, Erk, PLCҰЛ1,е’ STAT5ж°ҙе№іжҳҫи‘—еҸ—жҠ‘еҲ¶гҖӮ[1]PF-2341066 жҜҸеӨ©жҢ?00 mg/kgеүӮйҮҸеҸЈжңҚеӨ„зҗҶжҗәеёҰKarpas299 ALCL 移жӨҚзҳӨзҡ„SCID Beige е°Ҹйј пјҢе…·жңүжҠ—зҷҢй«ҳж•ҲжҖ§пјҢиҝҷз§ҚдҪңз”ЁеӯҳеңЁеүӮйҮҸдҫқиө–жҖ§пјҢеӨ„зҗҶ15еӨ©пјҢжүҖжңүиӮҝзҳӨе®Ңе…ЁиЎ°йҖҖгҖӮжӯӨеӨ? PF-2341066жҠ‘еҲ¶е…ій”®NPM-ALKдҝЎеҸ·и°ғиҠӮеҷ? еҢ…жӢ¬зЈ·и„Ӯй…¶C-ҰГ, дҝЎеҸ·иҪ¬еҜјеҷЁпјҢеҸҠиҪ¬еҪ•еӣ еӯ?, з»ҶиғһеӨ–дҝЎеҸ·и°ғиҠӮжҝҖй…? е’ҢAktзҡ„жҝҖжҙ»еүӮпјҢиҝҷдәӣдёҺ NPM-ALK зЈ·й…ёеҢ–е’ҢеҠҹиғҪеҸ—жҠ‘еҲ¶зӣёе…ігҖӮ[2] PF-2341066 жҠ‘еҲ¶йӘЁиӮүзҳӨзҡ„дёҖдәӣжҙ»еҠЁиЎҢдёәпјҢеҸҠе…¶иӮҝзҳӨз”ҹй•ҝ(дҫӢеҰӮ, еўһж®–е’Ңеӯҳжҙ?е’ҢиҪ¬з§ (дҫӢеҰӮпјҢе…Ҙдҫөе’ҢеҪўжҲҗе…ӢйҡҶ)гҖӮPF-2341066еҸЈжңҚйҘІе–ӮиЈёйј пјҢжҠ‘еҲ¶з”ҹй•ҝе’Ңзӣёе…ізҡ„йӘЁиӮүзҳӨиЈёйј з§»жӨҚзҳӨзҡ„йӘЁеҹәиҙЁзҡ„еҪўжҲҗгҖӮ[3] PF-2341066 жҢ?0 mg/kg еүӮйҮҸеӨ„зҗҶ c-MET-жү©еўһзҡ„GTL-16移жӨҚзҳӨпјҢеј•иө·иӮҝзҳӨиЎ°йҖҖпјҢиҝҷдё?8F-FDG ж‘„еҸ–зҡ„зј“ж…ўйҷҚдҪҺзӣёе…іпјҢдё”йҷҚдҪҺи‘Ўзі–зі–иҪ¬иҝҗиӣӢзҷҪ 1, GLUT-1зҡ„иЎЁиҫҫгҖӮ[4]
жҝҖй…¶е®һйӘӢь/b>
з”ҹеҢ–жҝҖй…¶е®һйӘӢъдҪҝз”Ёиҝһз»ӯиҖҰеҗҲзҡ„еҲҶе…үе…үеәҰжөӢе®ҡc-MetеӮ¬еҢ–жҙ»жҖ§пјҢйҖҡиҝҮеҲҶжһҗNADHж¶ҲиҖ—зҺҮиҖҢжөӢе®ҡc-MetиҜұеҜјзҡ„ADPдә§йҮҸпјҢиҝҷз§ҚдҪңз”Ёе…·жңүж—¶й—ҙдҫқиө–жҖ§гҖӮеңЁ 340 nmеӨ„дҪҝз”ЁеҲҶе…үе…үеәҰжі•еңЁжҢҮе®ҡж—¶й—ҙзӮ№жөӢе®ҡеҗёе…үеҖјзҡ„йҷҚдҪҺиҖҢи®Ўз®—NADHзҡ„ж¶ҲиҖ—йҮҸгҖӮдёәдәҶжөӢе®ҡKiеҖ? еңЁеҗ«е®һйӘҢиҜ•еүӮзҡ„е®һйӘҢеӯ”дёӯеҠ е…ҘдёҚеҗҢжө“еәҰPF-2341066пјҢ然еҗҺеңЁ37oCдёӢжё©иӮ?0еҲҶй’ҹгҖӮеҠ е…Ҙc-Metй…¶ејҖе§ӢиҝӣиЎҢе®һйӘҢеҸҚеә”гҖҒь/p>
з»Ҷиғһе®һйӘҢ
Cell lines: GTL-16иғғзҷҢз»Ҷиғһе’ҢT47Dд№іи…әзҷҢз»Ҷиғқь/p>
Concentrations: 0 nM-256 nM
Incubation Time: 1е°Ҹж—¶
Method:GTL-16иғғзҷҢз»Ҷиғһе’ҢT47Dд№іи…әзҷҢз»ҶиғһжҺҘз§ҚеңЁ96еӯ”жқҝдёҠпјҢеӯ”дёӯеҗ«еҹ№е…»еҹәпјҢеҹ№е…»еҹәдёӯеҗ«10% иғҺзүӣиЎҖжё?FBS)пјҢ然еҗҺиҪ¬з§»еҲ°ж— иЎҖжё…еҹ№е…»еҹәдё?b class="text-danger">еҗ?.04%зүӣиЎҖжё…иӣӢзҷ?BSA)пјҢеӨ„зҗ 24е°Ҹж—¶гҖ еңЁи°ғжҹҘй…ҚдҪ“дҫқиө–зҡ„RTK зЈ·й…ёеҢ–е®һйӘҢдёӯпјҢеҠ е…Ҙзӣёеә”зҡ„з”ҹй•ҝеӣ еӯҗпјҢеӨ„зҗ?0еҲҶй’ҹгҖӮз»Ҷиғһе’Ң PF-2341066е’?жҲ–йҖӮеҪ“й…ҚдҪ“еңЁжҢҮе®ҡж—¶й—ҙжё©иӮ?е°Ҹж—¶пјҢ然еҗҺдҪҝз”Ёеҗ« 1 mmol/L Na3VO4зҡ„HBSSеҶІжҙ—з»ҶиғһдёҖж¬?然еҗҺд»Һз»ҶиғһдёӯиҺ·еҫ—иӣӢзҷҪиЈӮи§Јзү©гҖӮйҡҸеҗ?йҖҡиҝҮеӨ№еҝғй…¶иҒ”е…Қз–«еҗёйҷ„иҜ•йӘҢжі•дҪҝз”Ёзү№е®ҡзҡ„жҚ•иҺ·жҠ—дҪ“ең?6еӯ”жқҝдёҠжөӢе®ҡйҖүе®ҡиӣӢзҷҪжҝҖй…¶зҡ„зЈ·й…ёеҢ–пјҢдҪҝз”Ёзү№зӮ№жЈҖжөӢжҠ—дҪ“жөӢе®ҡзЈ·й…ёеҢ–зҡ„й…Әж°Ёй…ёж®ӢеҹәгҖӮжҠ—дҪ“еҢ…иў«зҡ„е®һйӘҢжқ?a) еңЁиӣӢзҷҪиЈӮи§Јзү©еӯҳеңЁж—¶пјҢең?oCдёӢиҝҮеӨӣы(b)еңЁжә¶дәҺPBSзҡ?% Tween-20 дёӯеҶІжҙ?ж¬ ы(c)еңЁиҫЈж №иҝҮж°§еҢ–зү©й…¶ж Үи®°зҡ„жҠ—жҖ»зЈ·й…ёпјҲPY-20пјүжҠ—дҪ“пјҲ1:500пјүдёӯжё©иӮІ20еҲҶй’ҹ;(d) еҶҚж¬ЎеҶІжҙ—7ж¬ ы(e)ең?,3вҖ?5,5вҖ?еӣӣз”ІеҹәиҒ”иӢҜиғәиҝҮж°§еҢ–зү©й…¶еә•зү©дёӯжё©иӮІпјҢејҖе§ӢжҳҫзӨәеҸҚеә”пјҢеҠ е…Ҙ0.09 N H2SO4з»ҲжӯўеҸҚеә”; (f)ең?50 nm еӨ„дҪҝз”ЁеҲҶе…үе…үеәҰи®ЎжөӢе®ҡеҗёе…үеәҰгҖҒь/p>
(Only for Reference)
еҠЁзү©е®һйӘҢ
Animal Models: жҗәеёҰNCI-H441,жҲ–DLD-1,жҲ–MDA-MB-231зҡ„йӣҢжҖ§е’Ңйӣ„жҖ§nu/nuе°Ҹйј
Formulation: --
Dosages: 12.5 mg/kg/day, 25 mg/kg/day, е’?0 mg/kg/day
Administration: еҸЈжңҚеӨ„зҗҶ
(Only for Reference)
еҸӮиҖғж–ҮзҢ?/p>
еҸӮиҖғж–ҮзҢ?/b>
[1] Zou HY, et al. Cancer Res. 2007, 67(9), 4408-4417.
[2] Christensen JG, et al. Mol Cancer Ther. 2007, 6(12 Pt 1), 3314-3322.
[3] Sampson ER, et al. J Bone Miner Res. 2011, 26(6), 1283-1294.
[4] Cullinane C, et al. J Nucl Med. 2011, 52(8), 1261-1267.
[5] Gong HC, et al. Int J Proteomics. 2011, 2011, 215496.
[6] Zou HY, et al. Proc Natl Acad Sci U S A. 2015, 112(11):3493-8
е®үе…ЁдҝЎжҒҜ
 m.cnreagent.com
m.cnreagent.com