| е…ғзҙ еҗҚз§° |
й’ ь/span> |
е…ғзҙ з¬ҰеҸ· |
Ba |
еҺҹеӯҗеәҸж•° |
56 |
зӣёеҜ№еҺҹеӯҗиҙЁйҮҸ
(12C=12.0000) |
137.327 |
| иӢұж–ҮеҗҚз§° |
Barium |
| еҺҹеӯҗз»“жһ„ |
еҺҹеӯҗеҚҠеҫ„(?) |
2.78 |
еҺҹеӯҗдҪ“з§Ҝ(cm3/mol) |
39.24 |
з”өеӯҗжЁЎеһӢ |
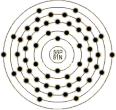
|
| з”өеӯҗжһ„еһӢ |
1s22s2p63s2p6d104s2p6d105s2p66s2 |
зҰ»еӯҗеҚҠеҫ„(?) |
1.35 |
| е…ұд»·еҚҠеҫ„(?) |
1.98 |
ж°§еҢ–жҖ?/span> |
2 |
| еҸ‘зҺ° |
1808е№ҙз”ұHumphry Davy е…Ҳз”ҹ(иӢұеӣҪпјҢдјҰж•?еҸ‘зҺ°гҖҒь/span> |
| е‘ҪеҗҚиө·жәҗ |
from 'barys' (Greek) - heavy |
| жқҘжәҗ |
еӯҳеңЁдәҺbarytine (BaSO4) зўій…ёй’Ўзҹҝ(BaCO3)дёӯпјҢз”ұдәҺеҸҚеә”жҙ»жҖ§еҫҲй«ҳпјҢиҮӘ然з•ҢжІЎжңүзәҜй’ЎгҖҒь/span> |
| з”ЁйҖ“ь/span> |
з”ЁдәҺзҒ«иҠұеЎһпјҢзңҹз©әз®ЎпјҢз„°зҒ«пјҢиҚ§е…үзҒҜгҖҒь/span> |
| зү©зҗҶжҖ§иҙЁ |
зҠ¶жҖ?/span> |
иҪҜзҡ„пјҢ银иүІйҮҚйҮ‘еұһгҖҒь/span> |
зҶ зӮ?в„? |
729 |
жІ зӮ?в„? |
1898 |
| еҜҶеәҰ(g/ccпј?00K) |
3.59 |
жҜ зғ?J/gK) |
0.204 |
и’ёеҸ‘зғ?KJ/mol) |
142 |
| зҶ”еҢ–зғ?KJ/mol) |
7.75 |
еҜјз”өзҺ?106/cm) |
0.03 |
еҜјзғӯзі»ж•°(W/cmK) |
0.184 |
| иҮӘзҮғзӮ?в„? |
- |
й— зӮ?в„? |
- |
|
|
| еҢ–еӯҰжҖ§иҙЁ |
|
| ең°иҙЁж•°жҚ® |
дё?nbsp; еә?/span> |
|
ж»һз•ҷж—¶й—ҙ(е№? |
10000 |
еӨӘйҳі
(зӣёеҜ№дә H=1Г—1012) |
123 |
| жө·ж°ҙдё?ppm) |
- |
ең°еЈі(ppm) |
500 |
еӨ§иҘҝжҙӢиЎЁйқЎь/span> |
4.7Г—10-3 |
| еӨӘе№іжҙӢиЎЁйқЎь/span> |
4.7Г—10-3 |
еӨ§ж°”(ppm(дҪ“з§Ҝ)) |
- |
еӨ§иҘҝжҙӢж·ұеӨғь/span> |
9.3Г—10-3 |
| еӨӘе№іжҙӢж·ұеӨғь/span> |
20.0Г—10-3 |
|
|
|
|
| з”ҹзү©ж•°жҚ® |
дәәдҪ“дёӯеҗ«йҮҺь/span> |
|
иӮ?ppm) |
0.04-1.2 |
| еҷЁе®ҳдё?/span> |
|
иӮҢиӮү(ppm) |
0.09 |
| иЎҖ(mg dm-3) |
0.068 |
ж—Ҙж‘„е…ҘйҮҸ(mg) |
0.6-1.7 |
| йӘ?ppm) |
3-70 |
дә?70Kg)еқҮдҪ“еҶ…жҖ»йҮҸ(mg) |
22 |
 m.cnreagent.com
m.cnreagent.com


 зЎқй…ёй’ ь/div>
зЎқй…ёй’ ь/div>